友情提示
本站部分转载文章,皆来自互联网,仅供参考及分享,并不用于任何商业用途;版权归原作者所有,如涉及作品内容、版权和其他问题,请与本网联系,我们将在第一时间删除内容!
联系邮箱:1042463605@qq.com
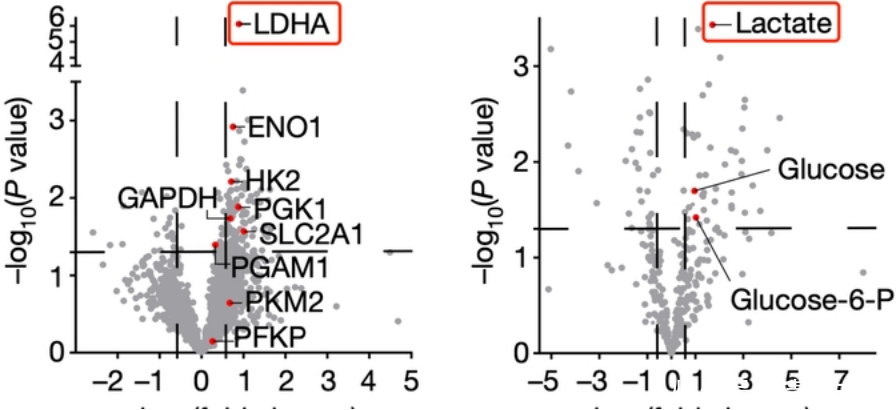
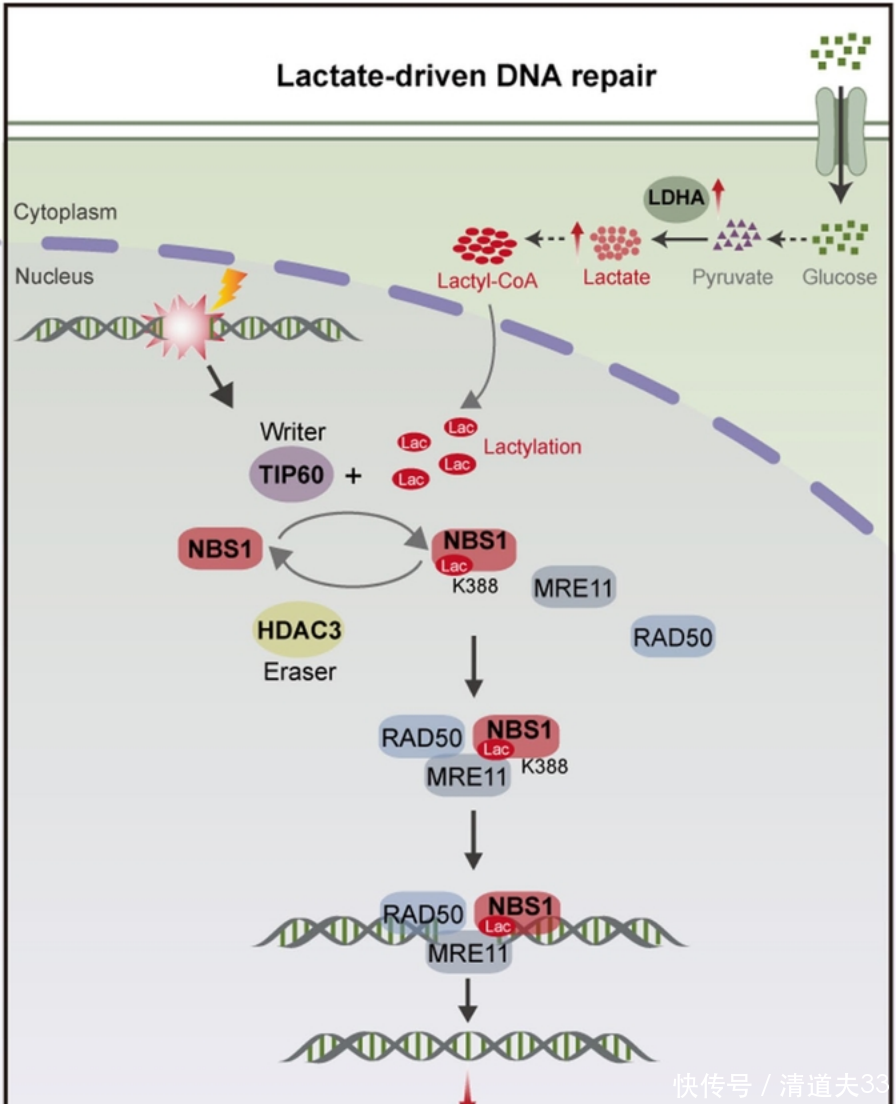
乳酸竟成癌细胞“保护伞”!中山大学团队发现,乳酸会促进癌细胞修复DNA损伤
25
0
相关文章
近七日浏览最多
最新文章
标签云
胃癌
胃炎
肿瘤
幽门
曹颖
萎缩性
手术
妇科
医生
腹腔包块
生育器官
医者仁心
郑大三附院
妇幼保健院
细胞治疗
天桥
济南市
肺癌
中药
成果库
中医药
神经系统疾病
恶性肿瘤
中山医院
治疗
演员
香港
周润发
刘嘉玲
陈荟莲
草蜢
乐队
梅艳芳
蔡一杰
男歌手
宝贝对不起
结节
张根硕
甲状腺癌
骨癌
症状
癌症
皮特
中英家庭
赵立坚
放化疗
皮肤瘙痒
胰腺癌
肺部
癌细胞
胸腔积液
声音嘶哑
不良习惯
调味料
健康
首都医科大学
医保
国家医保局
甲状腺激素
甲状腺
肝硬化
酒精肝
白酒
食管癌
预防肿瘤
肝脏
罹患癌症
鼻咽癌
放射治疗
宫颈癌
接种疫苗
肝癌
腹型肥胖
肠镜检查
肠道
饮食习惯
肠梗阻
济南
非小细胞肺癌
超声检查
航海家
饮食
牛肉
鸡蛋
槟榔
口腔癌
乳酸
血糖控制
肌肉
肌肉痉挛
血液循环
疾病
尿酸
高嘌呤食物
剧烈运动
痛风患者
痛风
睡眠质量
腿部肌肉
高尿酸血症
尿酸值
糖尿病
维生素d
运动能力
拉伸
关节
中山大学
科学家
睡眠时间
含糖饮料
黄金时间
乳酸菌
益生菌
营养物质
维生素b12
保健食品
肌肉群
五一
老年人
科技
果糖
海鲜
农科院
博士
浙江大学
清华大学
毕业院校
世界大学
本科
闫罗彬
副教授
白血病
西南大学
朱孔军
副部长
党委书记
广东省委
中央组织部
读博
兼职
离世
奖学金
复旦大学
人工智能
世界杯
李教授
清华
共产国际
莫斯科
苏联
风筝
旗开得胜
高校
985高校
深圳大学
投档线
暨南大学
录取通知书
无人机
傅园慧
跆拳道
刘伟
浙大
广东
指数
研究生
大手牵小手
爷爷奶奶
研究院
华南农业大学
香港科技大学
扫地机器人
华南理工大学
野鸡大学
大学
华南师范大学
老年痴呆
阿尔茨海默病
小米集团
减持
免疫治疗
基金会
股票
万军伟
小米
免疫
直肠癌
多肽
以色列
副作用
蒲公英根
是真的吗
药用价值
蒲公英
油炸食品
健康生活方式
免疫疗法
精神状态
慢性疾病
致癌物质
早餐
维生素c
柚子
黄曲霉素
优质蛋白
慢性萎缩性胃炎
胃黏膜
炎症
溃疡性结肠炎
医院
鉴定
疫苗
细胞
莴笋
抗氧化物
娃娃菜
黄花菜
四季豆
糖尿病人
血糖
红薯
盗汗
淋巴瘤
巴西
奥运会
宇航员
国际空间站
nasa
太空
结直肠癌
淋巴结肿大
力量训练
肠胃疾病
空气质量